Un innovador estudio publicado en la prestigiosa revista científica Cell Metabolism (IF=30,9) ha revelado un nuevo eje de señalización que conecta la microbiota intestinal, las células inmunitarias y los adipocitos progenitores, ofreciendo una nueva diana para la intervención en enfermedades metabólicas
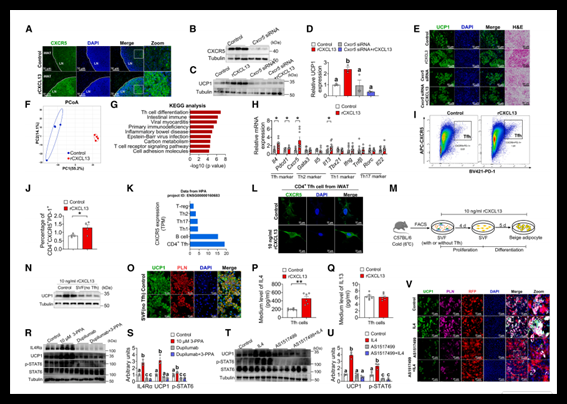
El estudio demuestra que la exposición al frío incrementa significativamente los niveles de Prevotella copri y de su producto metabólico, el ácido 3-fenilpropiónico (3-PPA), que activa la comunicación entre células inmunitarias y células progenitoras para favorecer la adipogénesis beige. Este proceso termogénico ayuda a combatir la obesidad.
La investigación pone de relieve el papel fundamental de las proteínas recombinantes de alta calidad para descifrar mecanismos biológicos complejos. En este caso, la compañía con sede en Wuhan Cloud-Clone Corp. proporcionó la herramienta clave para validar los hallazgos mediante su proteína recombinante CXCL13.
Un nuevo mecanismo metabólico: del intestino a la grasa
¿Cómo influye la microbiota intestinal en el gasto energético de una persona? Este estudio ofrece una nueva y prometedora respuesta.
El equipo investigador confirmó inicialmente que la eliminación de la microbiota intestinal perjudica la generación de grasa beige inducida por el frío. Sin embargo, la colonización intestinal con Prevotella copri restauró el efecto termogénico. El análisis metabolómico reveló que P. copri produce eficazmente una pequeña molécula metabolita: el ácido 3-fenilpropiónico (3-PPA).
La suplementación con 3-PPA reprodujo los beneficios metabólicos observados con la colonización de P. copri: favoreció el «pardeamiento» del tejido adiposo blanco inguinal (iWAT), aumentando la capacidad termogénica y el gasto energético en ratones, sin afectar a la función normal del tejido adiposo marrón clásico (BAT).
En términos más sencillos, el 3-PPA actúa como un «amplificador de la termogénesis», donde la exposición al frío funciona como el interruptor que potencia la señal responsable de transformar la grasa blanca en grasa beige generadora de calor.
El objetivo no son las células grasas, sino las «células madre de grasa»
Curiosamente, el 3-PPA no actúa directamente sobre los adipocitos maduros, sino que se dirige a las células progenitoras adipocitarias SMA⁺ (APCs), impulsando su diferenciación hacia células de grasa beige. Los experimentos de trazabilidad celular confirmaron que las células progenitoras SMA⁺ son la principal fuente de grasa beige inducida por el 3-PPA.
En los experimentos de intervención, la suplementación con 3-PPA en un entorno frío previno de forma significativa la obesidad y los trastornos metabólicos inducidos por una dieta rica en grasas. Este efecto dependía estrictamente de la exposición al frío, lo que subraya que el 3-PPA actúa como amplificador y no como desencadenante independiente. Además, este mecanismo fue verificado en células progenitoras adipocitarias humanas y en modelos porcinos, demostrando su potencial de aplicación entre distintas especies.
CXCL13: el puente inmunitario que conecta los metabolitos con la termogénesis de la grasa
¿Cómo activa el 3-PPA las células progenitoras adipocitarias? El análisis mecanístico condujo a un descubrimiento inesperado: el 3-PPA no afecta directamente a las células progenitoras, sino que primero activa un subconjunto de macrófagos similares a M2. El proceso se desarrolla del siguiente modo:
- El 3-PPA se une al receptor FFAR1 de los macrófagos, potenciando su metabolismo de fosforilación oxidativa.
- Esto induce la secreción de la quimiocina CXCL13, que recluta células T foliculares colaboradoras CXCR5⁺ (Tfh) hacia el tejido adiposo blanco.
- Las células Tfh secretan IL-4, activando la vía de señalización STAT6 en las células progenitoras SMA⁺ y promoviendo la adipogénesis beige.
Esta interacción entre células inmunitarias y células progenitoras forma una compleja red «inmunidad-células madre», donde macrófagos similares a M2, células Tfh y células progenitoras SMA⁺ colaboran para crear un microentorno inmunitario favorable para la formación de grasa beige. CXCL13 desempeña un papel central al conectar los metabolitos microbianos con la activación de las células progenitoras.
El valor de las herramientas de precisión: la proteína recombinante CXCL13 y la comprensión mecanística
Para aclarar el papel de CXCL13 en la generación de grasa beige, el equipo investigador utilizó CXCL13 recombinante altamente activa (CXCL13) en una serie de validaciones. Los resultados mostraron que, bajo condiciones estándar de diferenciación, CXCL13 no aumentaba directamente la expresión de UCP1 en adipocitos beige, confirmando que CXCL13 no actúa directamente sobre los adipocitos y proporcionando una base crítica para posteriores investigaciones mecanísticas.
Experimentos adicionales revelaron lo siguiente:
- CXCL13 incrementó significativamente la expresión de CXCR5 en los ganglios linfáticos de iWAT.
- La supresión de Cxcr5 mediante lentivirus bloqueó completamente el aumento de UCP1 inducido por CXCL13, confirmando que CXCR5 es el receptor esencial.
- Los análisis de RNA-seq y citometría de flujo confirmaron que tanto CXCL13 como 3-PPA aumentaban selectivamente los marcadores de células Tfh e incrementaban las células CD4⁺ Tfh en iWAT.
- Los experimentos de cocultivo aportaron la evidencia definitiva: CXCL13 promovía la formación de grasa beige únicamente en presencia de células Tfh. La eliminación de las células Tfh anulaba este efecto.
Gracias al uso de CXCL13, el equipo logró cartografiar toda la cadena de señalización: CXCL13 → células Tfh → IL-4 → generación de grasa beige.
Implicaciones y conclusiones: doble valor en descubrimiento mecanístico y aplicación tecnológica
Este estudio no solo descubre un nuevo mecanismo mediante el cual el 3-PPA regula la formación de grasa beige a través de la comunicación entre células inmunitarias y progenitoras, sino que también destaca el papel esencial de las proteínas recombinantes de alta calidad en la comprensión de procesos fisiológicos complejos. La aplicación rigurosa de CXCL13 permitió al equipo diferenciar entre efectos directos e indirectos, identificar las poblaciones celulares objetivo y confirmar la jerarquía de señalización.
Para investigadores especializados en metabolismo, inmunología y microbioma, seleccionar proteínas recombinantes de alta calidad y correctamente validadas es fundamental para profundizar en la exploración mecanística y garantizar la fiabilidad de las conclusiones.
Cloud-Clone: proteínas recombinantes de alta calidad para validación científica y aplicaciones traslacionales
En la validación de la generación de grasa beige mediada por CXCL13, la proteína recombinante CXCL13 de Cloud-Clone Corp. (RPB601Mu01) desempeñó un papel decisivo. El equipo investigador se apoyó en esta proteína altamente activa para mapear con precisión el eje de señalización CXCL13 → células Tfh → IL-4 → generación de grasa beige, estableciendo a CXCL13 como el mediador inmunitario central que conecta los metabolitos microbianos con la termogénesis.
Cloud-Clone ofrece:
- Más de 17.000 proteínas recombinantes, cubriendo múltiples especies, incluidos humanos, ratones, ratas y cerdos.
- Plataformas de expresión y purificación de proteínas, así como modificación de antígenos de pequeñas moléculas, permitiendo producción a gran escala mediante biorreactores para satisfacer necesidades industriales.
- Más de 1.000 proteínas activas, incluidas citocinas (TGF-β1, TNF-α, IL-2), factores de crecimiento (GM-CSF, EGF), enzimas (peroxidasa, acetil heparinasa, ADN polimerasa) y objetivos IVD (AMH, PINP).
- Estricta validación de actividad: todas las proteínas se someten a múltiples ensayos biológicos para garantizar estabilidad y fiabilidad tanto en investigación básica como en aplicaciones traslacionales.
Tanto para la exploración de mecanismos avanzados como para el desarrollo de reactivos diagnósticos y terapias, Cloud-Clone mantiene su compromiso de proporcionar a investigadores de todo el mundo proteínas recombinantes fiables y consistentes entre lotes.
Referencia
Cell Metab. 2026 Apr 7;38(4):763-778.e7.
DOI: 10.1016/j.cmet.2026.01.017. Epub 2026 Feb 24.
«Microbial-derived 3-phenylpropionic acid orchestrates immune-progenitor cell crosstalk to promote beige adipogenesis and energy expenditure.»
Sobre Cloud-Clone Corp.
Cloud-Clone Corp. está especializada en el desarrollo y producción de reactivos de inmunoensayo de alta calidad y soluciones de detección. Con un enfoque centrado en la ingeniería de anticuerpos, el desarrollo de ensayos multiplex y la compatibilidad multiplataforma, la compañía proporciona herramientas de investigación diseñadas para respaldar la medicina de precisión y la investigación biomédica avanzada a nivel global.
Sus principales productos y servicios incluyen el desarrollo de proteínas, anticuerpos, kits ELISA, células primarias y kits de ensayos multiplex, así como servicios profesionales CRO para satisfacer las diversas necesidades de la investigación biomédica y sectores relacionados.
Para más información sobre Cloud-Clone Corp., visitar www.cloud-clone.com.
• LinkedIn de Cloud-Clone Corp.
• Instagram de Cloud-Clone Corp.